Durante décadas asumimos que el envejecimiento era un proceso lineal, acumulativo e inevitable. Hoy, la biología está cuestionando ese paradigma. La epigenética —el sistema de marcas químicas que regula qué genes se activan o silencian— se ha convertido en uno de los territorios más prometedores de la medicina de longevidad.
Lo que antes parecía ciencia ficción comienza ahora a entrar en fase clínica: la reprogramación epigenética parcial ya se está probando en humanos.
El origen del concepto: resetear sin borrar la identidad
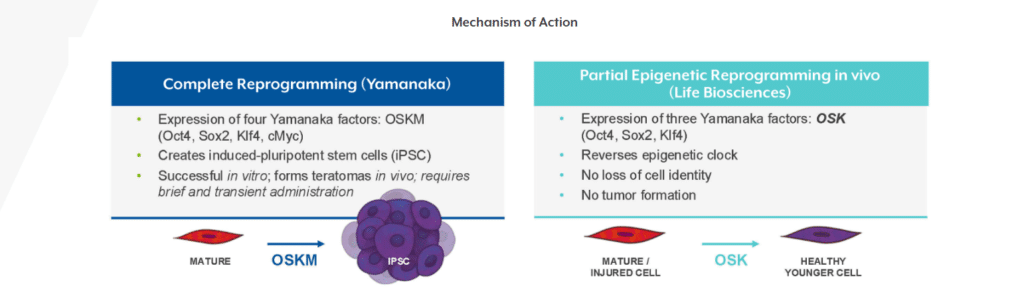
La reprogramación celular se hizo mundialmente conocida con el descubrimiento de los factores de Yamanaka (OCT4, SOX2, KLF4 y c-MYC), capaces de convertir células adultas en células madre pluripotentes inducidas (iPSCs). Este proceso borra la identidad celular y reinicia el estado biológico a una fase embrionaria.
El problema: una reprogramación completa implica pérdida de función especializada y riesgo de tumorigenicidad.
La solución que emerge en la última década es la reprogramación parcial: activar temporalmente algunos factores (habitualmente OCT4, SOX2 y KLF4, sin c-MYC) para rejuvenecer el epigenoma sin desdiferenciar la célula.
En modelos animales, esta estrategia ha:
- Restaurado visión en ratones con daño del nervio óptico
- Mejorado función tisular en tejidos envejecidos
- Reducido la edad epigenética medida por relojes moleculares
- Aumentado parámetros de salud en modelos de envejecimiento acelerado
El hallazgo clave es que la información de juventud parece conservarse en el epigenoma, y puede ser reactivada.
En 2026, la FDA autorizó el inicio del primer ensayo clínico en humanos basado en esta tecnología. El tratamiento se denomina ER-100, desarrollado por Life Biosciences.
Este estudio de fase 1 evalúa seguridad y señales preliminares de eficacia en pacientes con:
- Glaucoma de ángulo abierto
- Neuropatía óptica isquémica anterior no arterítica (NAION)
Ambas patologías implican degeneración de las células ganglionares de la retina y daño progresivo del nervio óptico.
¿En qué consiste exactamente ER-100?
ER-100 es una terapia génica de administración local intraocular que utiliza un vector viral adenoasociado (AAV) para introducir en las células un conjunto controlado de factores de reprogramación:
OCT4, SOX2 y KLF4 (OSK)
Estos factores no modifican el ADN en sí, sino que reorganizan las marcas epigenéticas (metilación del ADN, remodelación de cromatina, modificaciones de histonas), restaurando patrones de expresión génica más juveniles.
Elemento diferencial crítico: control temporal
Uno de los aspectos más sofisticados del diseño es que la expresión de los factores está bajo un sistema inducible, activable mediante doxiciclina. Esto permite:
- Activar la reprogramación durante un tiempo limitado
- Detenerla si aparecen efectos adversos
- Minimizar riesgo de desdiferenciación
Este control temporal es una de las principales diferencias frente a intentos previos de reprogramación más agresiva.
¿Por qué empezar por el ojo?
La elección no es casual.
El entorno ocular ofrece ventajas estratégicas:
- Es un compartimento relativamente aislado (menor exposición sistémica).
- Permite administración local precisa.
- La función visual es medible con biomarcadores objetivos.
- Existen sólidos datos preclínicos en modelos animales.
En primates no humanos, la expresión de OSK restauró patrones epigenéticos juveniles y mejoró función neuronal tras daño óptico.
El ojo funciona aquí como modelo de prueba controlado para validar seguridad biológica antes de plantear aplicaciones sistémicas.
¿En qué se diferencia ER-100 de otros enfoques de longevidad?
La mayoría de intervenciones actuales en longevidad actúan sobre consecuencias del envejecimiento:
- Senolíticos → eliminan células senescentes
- Metformina o rapamicina → modulan vías metabólicas
- NAD+ boosters → apoyan metabolismo mitocondrial
- Terapias hormonales → restauran niveles decrecientes
ER-100 es conceptualmente distinto:
no modula el daño, intenta restaurar la programación celular original.
Es una intervención aguas arriba, sobre la arquitectura epigenética que regula múltiples procesos biológicos simultáneamente.
Eso la sitúa en una categoría potencialmente transformadora.

Potencial clínico si los resultados son positivos
Si se demuestra seguridad y eficacia funcional, las implicaciones serían profundas:
1. Neurodegeneración
Podría abrir una vía para enfermedades como Parkinson o Alzheimer, donde la disfunción epigenética contribuye a la pérdida neuronal.
2. Regeneración tisular
Restaurar función en tejidos con baja capacidad regenerativa (corazón, retina, sistema nervioso).
3. Medicina preventiva del envejecimiento
Rejuvenecer perfiles epigenéticos antes de que aparezca patología manifiesta.
4. Biomarcadores de edad biológica
Validar relojes epigenéticos como herramientas clínicas para medir reversión real del envejecimiento.
Estamos hablando de intervenir sobre el denominador común de múltiples enfermedades relacionadas con la edad.
Riesgos y prudencia científica
El entusiasmo debe equilibrarse con cautela.
Riesgos potenciales incluyen:
- Activación oncogénica
- Inestabilidad epigenética
- Respuesta inmunitaria al vector viral
- Efectos no previstos a largo plazo
La fase 1 está centrada en seguridad. No busca demostrar rejuvenecimiento sistémico, sino establecer que el procedimiento es viable en humanos.
Un cambio de paradigma en salud y bienestar
Desde la perspectiva del bienestar y la longevidad, este ensayo marca un punto de inflexión. Por primera vez, la hipótesis de que el envejecimiento es biológicamente reversible se está evaluando bajo supervisión regulatoria formal.
No estamos ante un suplemento, ni ante una intervención cosmética molecular. Estamos ante la posibilidad de que el epigenoma —ese sistema dinámico que organiza nuestra identidad biológica— pueda reprogramarse de forma controlada.
Si la seguridad se confirma y aparecen señales funcionales positivas, el impacto podría redefinir la medicina del siglo XXI: pasar de tratar enfermedades individuales a restaurar la juventud funcional de los tejidos.
El reloj biológico ya no parece tan inmutable.






